记者 | 陈杨
编辑 | 谢欣
11月1日,国家药监局(NMPA)发布公告,决定统一修订注射用黄芪多糖、灯盏花素氯化钠注射液和板蓝根注射液说明书中的警示语及不良反应、禁忌和注意事项。
具体而言,上述三类药物说明书均应增加警示语,内容包括:本品不良反应包括过敏性休克,应在有抢救条件的医疗机构使用,使用者应接受过过敏性休克抢救培训,用药后出现过敏反应或其他严重不良反应须立即停药并及时救治。另外,灯盏花素氯化钠注射液说明书应增加的警示语还包括:脑出血急性期或有出血倾向的患者禁用。
据NMPA官网信息,黄芪多糖、灯盏花素氯化钠注射液分别为天津赛诺制药、通化天实制药的独家产品。板蓝根注射液则有37条批文,涉及企业包括葵花药业、云南白药、神威药业、亚宝药业、科伦药业、华润三九、云南生物谷等多家上市公司。而以“板蓝根”检索,共可得到1193条批文,除注射液外,还包括片剂、颗粒、糖浆等。其中,板蓝根颗粒977条,复方板蓝根颗146条,为主要剂型。
板蓝根的主要成分是十字花科植物菘蓝的干燥根,功能主治为清热、解毒凉血,用于风热感冒、咽喉肿痛等。实际上,作为“国民神药”,板蓝根几乎从未在以往的各种传染病疫情中缺席,不过,对其疗效和安全性的质疑也始终存在。
早在1988年,上海爆发甲肝疫情,当时的扬子江制药厂加急制药,生产出385万包板蓝根干糖浆援护,掌舵人徐镜人也因此获得了“板蓝根大王”的名号。

而板蓝根彻底名声大噪是在2003年的“非典”期间。当年4月,国家中医药管理局制定《非典型肺炎中医药防治技术方案(试行)》,针对与非典病例或疑似病例有接触的健康人群,给出了包括板蓝根的预防处方。5月下旬,全国防治非典型肺炎指挥部科技攻关组宣布,包括板蓝根冲剂在内的8个中成药能够明显改善非典不同病理环节的症状。
此后,2003年的H7N9型禽流感、2009年的甲型H1N1流感期间,板蓝根多次遭到哄抢、断货。2017年,香雪制药的板蓝根还成功出海,获得英国药品和健康产品管理局(MHRA)的注册批件。
而在新冠疫情中,虽然早在2020年1月,国家卫健委官方微博健康中国已辟谣板蓝根用于新冠肺炎预防的说法,该药还是“虽迟但到”。
2020年10月,中国工程院院士钟南山在报告中称,经过抗新冠病毒的体外药效筛选,发现白云山复方板蓝根颗粒显示出体外抑制药效。随后板蓝根再遭哄抢。白云山后发布告澄清,上述“抑制药效”仅是体外实验结果,后续还需对该产品开展进一步相关工作。而与众多因 “体外实验结果”出圈的药物一样,时至今日,中国临床试验注册中心官网上也检索不到板蓝根针对新冠肺炎的临床试验信息。
此外,近年来,多个剂型的板蓝根制剂先后由处方药、双跨药转变为非处方药,也使其在宣传、销售和使用上获得了更多的自由空间。米内网的数据显示,2019年,板蓝根颗粒、复方板蓝根颗粒在国内城市零售药店的销售额分别为10.65亿元、4.30亿元。
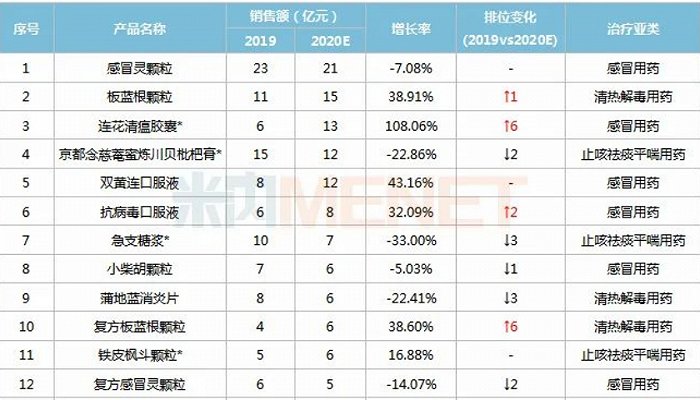
受疫情影响,2020年国内城市零售药店终端呼吸系统中成药销售规模下滑,但预计板蓝根颗粒、复方板蓝根颗粒的销售额分别为15亿元、6亿元,增长率均约为38%,分别位居该品类销售额第2名和第10名。
 图片来源:米内网
图片来源:米内网
不过,与热销对比鲜明的是,近几年,国家对板蓝根的监管趋严。2018年3月,国家药典委员会发布《关于板蓝根颗粒质量标准拟增修订的公示》,修订了板蓝根颗粒的制法、鉴别等内容,并增加了含量测定项。
同年11月,医政医管局发布《流行性感冒诊疗方案(2018年版修订版)》,其中已不见板蓝根的身影。对此,据《南方都市报》的报道,中山大学附属第一医院儿科专家张洪宇认为,板蓝根未被列入指南主要是因为,目前从一些临床循证研究来看,板蓝根对于病毒性流感作用有限。
同时,本次也非板蓝根产品首次修订说明书。2021年4月,NMPA将复方板蓝根颗粒由处方药转化为非处方药,其说明书一并修订。其中首次列出了该药有腹泻、腹痛、恶心、呕吐、腹部不适、瘙痒、皮疹、头晕、过敏反应等不良反应报告,并在【注意事项】中加入“发热体温超过38.5摄氏度的患者,应去医院就诊”的内容。
此外,板蓝根颗粒的原料板蓝根饮片也一直是不合格饮片的重灾区。2017年2月,原国家食药监总局发布的《总局关于54批次中药饮片不合格的通告(2017年第21号)》显示,在54批不合格的中药饮片中,板蓝根不合格数为28批次,占一半以上。
2019年,国际标准化组织(ISO)发布《中医药-板蓝根药材》国际标准,对板蓝根在种植产地,干燥、运输,包装,农药和重金属残留等方面进行同质化规定。中药材是中药饮片的原料,指原植物、动物、矿物除去非药用部位的商品药材。对原料的质量规范在一定程度上或可改善饮片的质量问题。
:点击
(xxx)评论